杭州CRO服务商
众多企业在医疗器械研发过程中踩坑不断,损失惨重。研发规划中,看到竞争公司做什么产品,就去生产一个同类产品;看到市场上什么产品卖得好,就跟着研发生产,产品线不清晰,不成体系。短期可能会吃到市场红利,但是久而久之,缺乏对临床需求和行业方向的把握,只会跟风分配企业资源进行研发的企业是难以长久发展下去的,终究会被行业残忍淘汰。思脉得医疗科技集团依托自身行业资源,从用户需求、法规要求、质量要求、成本要求及市场需求多个维度为客户进行定制化的设计开发服务,将有限的企业资源发挥出成效。在医疗器械产品设计中,市场调研和用户反馈是不可忽视的环节。杭州CRO服务商

在2019年4月,国家药品监督管理局印发《关于实施中国药品监管科学行动计划的通知》,围绕“创新、质量、效率、体系、能力”主题,推动监管理念创新,开展药品监管科学研究。针对新时期药品、医疗器械和化妆品监管存在的突出问题,通过创新监管工具、标准和方法,进一步增强监管工作的科学性、前瞻性和适应性,更好满足新时代公众对药品的需求。对安全的新需求。设计和开发输入是研发过程的重要组成部分。针对其在法规和质量管理体系方面的要求,加强对行业现状和监管新方法的研究,进一步明确要求,切实加大投入力度,提高设计开发输入的合规性、一致性。医疗器械的维修CDMO(医疗器械制造和开发外包服务)在医疗行业中的地位逐渐崭露头角。
医疗器械生产质量管理规范植入性医疗器械实施细则和检查评定标准,第五章设计和开发的具体要求(主要包括设计开发评审和验证)如下:第三十六条生产企业应当在设计和开发的适宜阶段安排评审,保持评审结果及任何必要措施的记录。第三十七条生产企业应当对设计和开发进行验证,以确保设计和开发输出满足输入的要求,并保持验证结果和任何必要措施的记录。第三十八条生产企业应当对设计和开发进行确认,以确保产品满足规定的使用要求或预期用途的要求,并保持确认结果和任何必要措施的记录。确认可采用临床评价和/或性能评价。进行临床试验时应当符合医疗器械临床试验法规的要求。
众所周知,二三类医疗器械产品的研发周期长,且失败风险高,对于大多数中小企业来说门槛很高,行业内众多产品市场长期被大型公司垄断。随着医疗器械MAH制度的落实,专人做专事的经营理念被不断宣传,制度鼓励企业将临床前研究、临床试验、生产制造、经销配送等环节外包给其他企业,如此一来,不仅避免了资源的浪费,还将促进研发型、代工型、销售型企业各尽其能,做精做专,促进各类型企业向产业化、规模化发展。思脉得作为一家全球医械企业值得信赖的技术服务商,拥有专业的技术开发团队,技术涉及领域涵盖光电技术、精密机械、软件开发、电路设计等等。CDMO服务商在器械CDMO赛道上不断探索盈利模式,为企业提供更多选择。
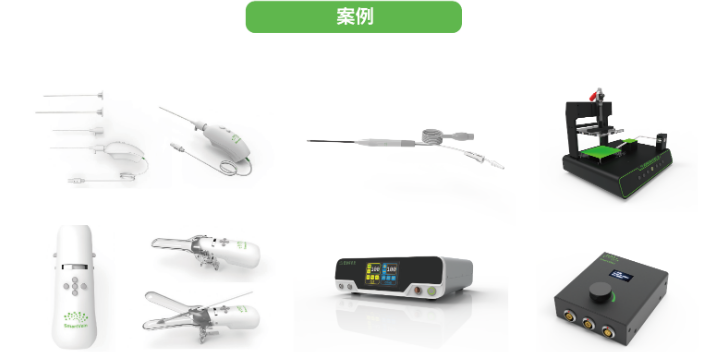
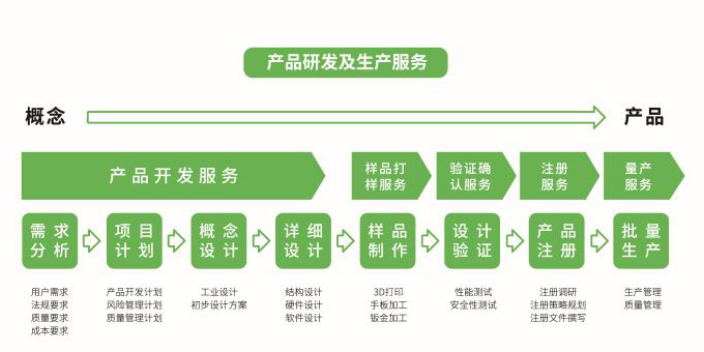
随着医疗大健康行业的快速发展,越来越多的企业意图进军医疗器械行业,但是面对错综复杂的法规要求、标准严苛的生产环境、价格高昂的研发设备、人才紧缺的开发团队。想要真正入行的门槛并不低,那就入不了行了么,当然不是。思脉得医疗科技集团秉承创新技术及服务,为客户提供超预期价值为宗旨,致力于为医疗行业客户提供全套技术解决方案,为不同客户提供定制型的设计开发服务,具体涵盖产品需求分析、项目计划、概念设计、详细设计、样品制作、设计验证、产品注册等。医疗器械设计必须符合FDA等监管机构的法规,确保产品上市合规。杭州一站式CMO服务商
CDMO支持企业将研究成果转化为有市场竞争力的医疗器械产品。杭州CRO服务商
医疗器械设计开发输入为产品开发提供产品性能参数要求、临床需求、工艺路线、风险因素识别、性能评价支持数据、市场条件等信息,这些信息直接决定了产品整个生命周期中输入、验证、确认和生产过程的运行情况。设计开发输入在产品研发和监管工作中的重要性日益凸显,行业对输入要求的理解和应用要求也越来越高。在市场监管法规的指导下,中小企业想要在医疗器械设计开发领域进行长足的发展,可以借助第三方技术服务公司进行进行委托设计开发或者定制开发,从而有效的避免设计开发中产生的风险隐患。杭州CRO服务商
上一篇: 杭州一站式CMO服务商
下一篇: 杭州内窥镜OEM代加工